- 翰林提供學術活動、國際課程、科研項目一站式留學背景提升服務!
- 021-63526630
IB物理課程真題講解: 比潛熱、理想氣體
IB物理課程真題講解: 本題是 2017 年 IB 物理試卷 paper 2 的一道大題,在 SL 和 HL 的試卷中,這道題基本沒什么區別,所以適用于所有考 IB 物理的學生。這道題主要涉及到了功率、比潛熱、和理想氣體的知識,具體講了液氧蒸發成氧氣的過程。
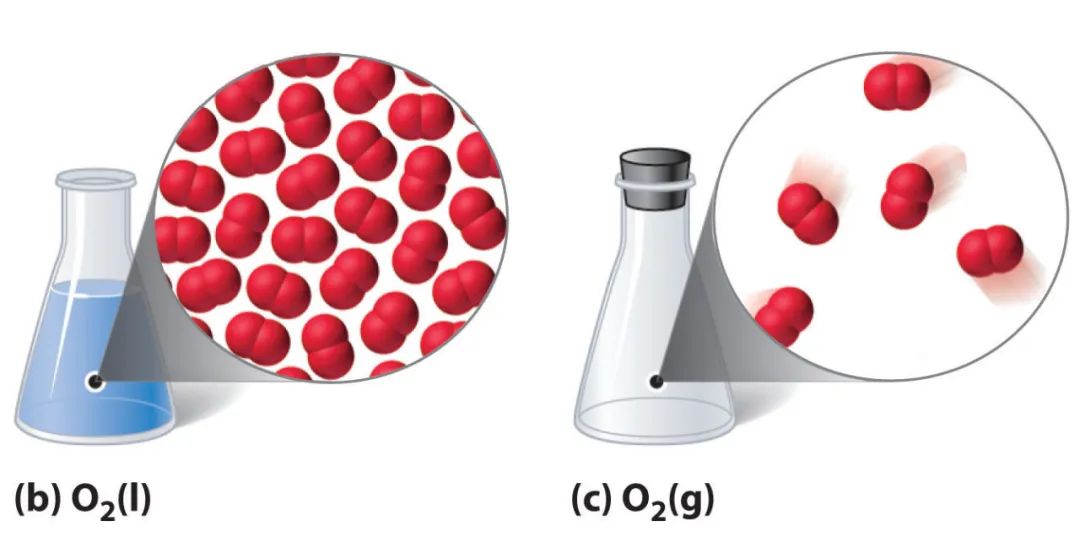
如下圖所示,一個氧分子是由兩個氧原子組成,是雙原子分子 (diatomic molecule)。液氧(左圖)的分子結構比較緊密,分子之間作用力明顯;而蒸發成氧氣后(右圖),分子之間的間距非常遠,分子之間作用力隨之變得微弱。
我們在做 IB 物理大題時,一定要看每一小問的分值情況,如果是 [1] 分的小問,說明只有一個得分點,沒必要寫太多、浪費時間;如果是 [4] 分的小問,就對應四個得分點,需要認真對待,至少也得寫出四個方面來覆蓋到四個得分點。這是答題中的技巧。
下面看題吧,希望你先嘗試著自己完成這道題,自己思考、做完一遍后,再看后面的答案解析。答案解析中標注 "✔️ " 的位置,表示此處得 1 分。
Liquid oxygen at its boiling point is stored in an insulated tank.? Gaseous oxygen is produced from the tank when required using an electrical heater placed in the liquid.
The following data are available.
Mass of 1.0 mol of oxygen = 32 g
Specific latent heat of vaporization of oxygen =?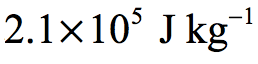
(a) Distinguish between the internal energy of the oxygen at the boiling point when it is in its liquid phase and when it is in its gas phase.? [2]
(b) An oxygen flow rate of 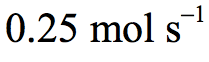 ?is needed.
?is needed.
(i) Calculate, in kW, the heater power required.? [2]
(ii) Calculate the volume of the oxygen produced in one second when it is allowed to expand to a pressure of 0.11 MPa and to reach a temperature of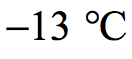 .? [2]
.? [2]
(c) State one assumption of the kinetic model of an ideal gas that does not apply to oxygen.? [1]
答案解析:
(a) 問中考察了處于沸點的氧,其液態和氣態內能的區別。該小問共兩分,第一個得分點是解釋一下內能是所有分子勢能和動能的和,即:
Internal energy is the sum of all the potential energy and kinetic energy of the molecules of the oxygen. ✔️
第二點則可以針對 “沸點” ,處于沸點的液氧被加熱是一個相變過程,相變過程的特點是溫度不變,所以動能不變;加熱所輸入的能量用來打破液氧之間的 bonds,使氧分子之間相互遠離,成為氣態氧分子,勢能增加了。動能不變,勢能增加,所以氣態氧分子的內能比液氧大。這些解釋又可以寫出如下兩個得分點:
At boiling point, the average kinetic energy of molecules in liquid and gas is the same ✔️
Gas has a higher internal energy than liquid ✔️
以上三個得分點寫出兩個即可。
(b) (i) 問告訴了我們單位時間 (即 1 秒鐘) 需要 0.25 mol 的氧氣,要求加熱器的功率。由于功率是單位時間內加熱器輸入的熱量,不妨先將功率進行展開: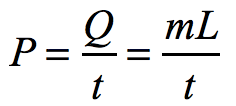
上式中,熱量 Q 用來使液氧發生相變,所以有 Q = mL,式中 L?= 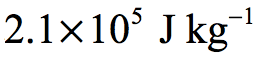 ,是液氧的比潛熱。想求 P,下面就要解決上式中的 m / t。由于已知中涉及到摩爾數 n 和摩爾質量 μ,可將液氧質量 m 展開,有:
,是液氧的比潛熱。想求 P,下面就要解決上式中的 m / t。由于已知中涉及到摩爾數 n 和摩爾質量 μ,可將液氧質量 m 展開,有: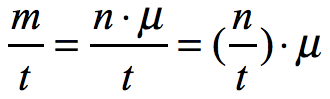
式中 n / t = 0.25 mol/s, μ = 32 g/mol,均為已知,代數計算可得: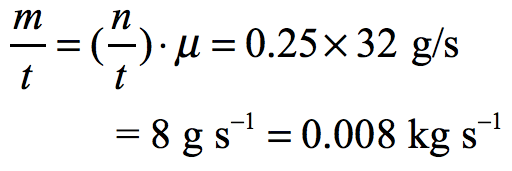 ✔️
✔️
注意上式中需要把結果化為國際單位制,即 kg / s,據此得到 1 分。接下來將該結果代入到上面功率 P 的表達式中、計算,即可得到第 2 分: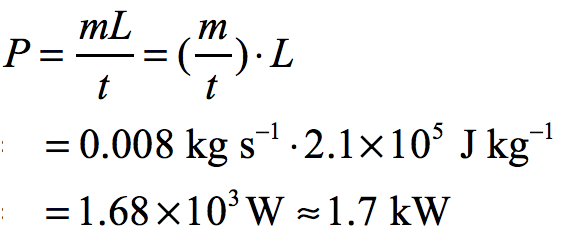 ✔️
✔️
結果需注意兩點:一是題目中已知的有效數字是 2 位,所以結果中要約為 2 位有效數字;二是本小問明確要求以 “kW”?這個單位呈現結果,不要忘記。
(b) (ii) 小問中涉及到體積 V,壓強 p,以及 溫度 T 這三個物理量,十有八九是在考察理想氣體狀態方程:pV = nRT 。由于式中的 T 是絕對溫度,單位是 “K”,所以第一件要做的事是將 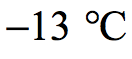 轉換為 “K” 這個單位:
轉換為 “K” 這個單位: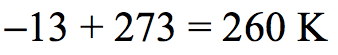 ✔️
✔️
接下來就是根據題目中的問題來對 pV = nRT 進行變換、代數求解。題中要求單位時間 (每秒) 內產生氧氣的體積,即 V / t ,那么我們不妨將 pV = nRT 兩端同除以時間 t,湊出 V / t 這個物理量: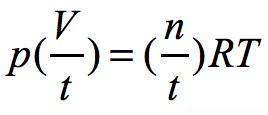
左式中,壓強 p 是已知;右式中,單位時間內產生氧氣的摩爾數 n / t 、氣體常數 R、絕對溫度 T 均為已知,代入上式即可求出結果: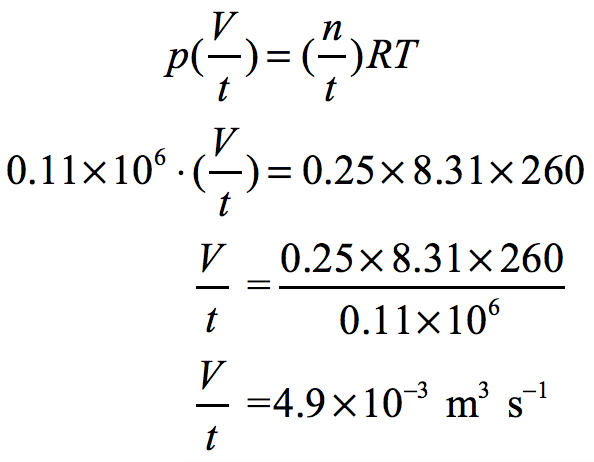 ✔️
✔️
(c) 問主要考察了理想氣體運動模型的幾個假設,這些假設中的哪一個都不能適用于實際氣體,最多只是一個近似,所以只要寫出其中一個即可。下面我列出五個主要的,需要同學們背一下:
The molecules are point particles, each with negligible volume?✔️
No intermolecular?forces between gas?particles?✔️
Ideal gas cannot be liquefied or solidified ✔️
The collisions of?the particles with each other and with the container walls?are?elastic?✔️
Ideal gas assumes monatomic particles ✔️
掃碼添加翰林顧問老師,可一對一制定國際課程規劃
【免費領取】IB/IBDP 備考資料合集~


最新發布
? 2026. All Rights Reserved. 滬ICP備2023009024號-1









