- 翰林提供學術活動、國際課程、科研項目一站式留學背景提升服務!
- 021-63526630
IGCSE 化學題型分析-真題講解
在 IGCSE 化學考試中,計算題雖占據的比重不大,但一定要拿滿分的題目。
在這個階段,計算題只會與摩爾質量這個知識點相關,也就意味著學生需要掌握的相關知識點不多,也相對較淺。
那什么是摩爾質量呢?和它相關的考試計算題又會是什么樣的呢?答題需要注意什么技巧?
摩爾是什么呢?
其實,我們只要把他當做一個計算物質的量的單位就行(1 摩爾 = 1 mol )。所謂的單位,事實上也都是人們為了方便計算所設定的。比如我們去包子店跟老板說,給我來一打包子,這其中的一打,也就是 12 個,就是我們方便溝通計算所設定的單位。
1 摩爾的任意物質,其所包含的粒子數為 6.02 X 10^23 (阿伏伽德羅常數 NA)個。這里有必要解釋一下什么是粒子,粒子( Particles )是組成物質的基本獨立個體,電子,質子,中子,原子,分子都可以被稱為粒子。比如 1 摩爾的水就包含 6.02 X 10^23 次方個水分子,1 摩爾的鐵就包含 6.02 x 10^23 次方個鐵原子(鐵是由鐵離子和自由電子組成的晶體結構,此處贊稱鐵原子。)
通過實驗和測試,我們將物質的量(mol)定義為,1 mol 的任意物質,其質量,以克為單位,數字上等于這個物質的相對式量(相對原子或者分子質量),比如 1 摩爾的 H?O,其質量就等于 18g,1 摩爾的氫氣(H?),其質量就等于兩個 H 原子的質量,2g。
由此,我們就有了物質的量與物質的質量之間的關系:
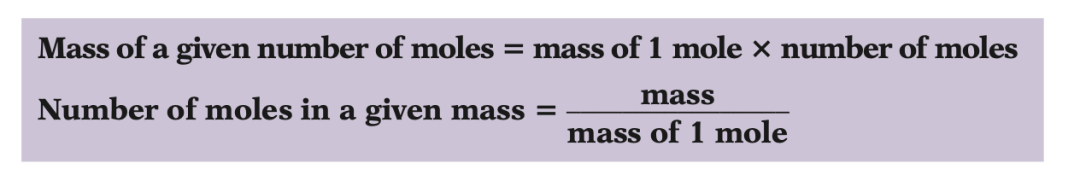
求一個物質的物質的量(How many moles)等于這個物質的質量,除去 1 摩爾此物質擁有的質量,也就是物質的總重量除去其相對式量。

第六題,題目要求我們找到 3 mole ethanol,C?H?OH 的質量。首先我們先計算出 C?H?OH 的相對分子質量(C:12 ;H:1;O:16),是 46 。也就是說 1 mol 的 C?H?OH 質量應該是 46 g,那么 3 mol 的 C?H?OH 就應該是 3 x 46 ,也就是 138 g。
備考IGCSE,刷題資料必不可少,掃碼咨詢
【免費領取】歷年真題及解析,考前沖刺,名師講解,專業答疑!

以上就是關于【IGCSE 化學題型分析-真題講解】的解答,如需了解學校/賽事/課程動態,可至翰林教育官網獲取更多信息。
往期文章閱讀推薦:
從競賽到華爾街!量化巨頭最愛院校曝光:MIT斷層第一,滑鐵盧成黑馬!
直播預告 | 碩博導師分享數學競賽規劃路徑!丘獎/ISEF全解析!

最新發布
? 2026. All Rights Reserved. 滬ICP備2023009024號-1









