- 翰林提供學(xué)術(shù)活動(dòng)、國(guó)際課程、科研項(xiàng)目一站式留學(xué)背景提升服務(wù)!
- 021-63526630
化學(xué)學(xué)習(xí)方法從AS到A2如何真正學(xué)懂Equilibirum
小提示:本文干貨較多,請(qǐng)耐心并認(rèn)真閱讀對(duì)于Equilibrium的知識(shí)相信同學(xué)們無(wú)論在GCSE 還是在AL階段都有一定程度的了解,并且在我們的印象中這并不是一個(gè)特別難懂或者難得分的知識(shí)點(diǎn)。
你以為知道Dynamic equilibrium 就夠了?
知道怎么去判斷Equilibrium shift就夠了?
知道如何去求解兩個(gè)Equilibrium constant就夠了?
如果你這么想就太天真了!
在階段,你要明白:
Chemical Equilibrium is an Dynamic Equilibrium,相信同學(xué)們對(duì)于這句話已經(jīng)耳熟能詳,沒(méi)錯(cuò),它告訴我們的就是化學(xué)平衡是一個(gè)動(dòng)態(tài)平衡。
但是大部分同學(xué)們只是停留在這句話的背誦上,而沒(méi)有真正的考慮它在真正告訴我們什么。
其實(shí)對(duì)于動(dòng)態(tài)平衡的理解要從這兩個(gè)方面出發(fā):
第一,當(dāng)我們說(shuō)一個(gè)chemical reaction reaches equilibrium的時(shí)候,那么作為一個(gè)reversible reaction,rate of forward reactionrate of backward reaction。
也就是說(shuō),在可逆反應(yīng)當(dāng)中,當(dāng)一個(gè)反應(yīng)達(dá)到平衡之后,有多少反應(yīng)物轉(zhuǎn)化為生成物就有多少生成物轉(zhuǎn)化回反應(yīng)物。
第二,當(dāng)我們說(shuō)一個(gè)chemical reaction reaches equilibrium的時(shí)候,the concentrations of all the substance in the reaction stay the same. 注意,同學(xué)們對(duì)于這個(gè)same的理解有時(shí)候會(huì)出現(xiàn)偏差。
它指的并不是所有物質(zhì)的concentration 都相等(equal)!而是在說(shuō)當(dāng)反應(yīng)達(dá)到平衡的時(shí)候,the concentrations of all the substance in the reaction stay unchanged!
每一個(gè)substance 在平衡的時(shí)候都有自己的concentration并且這個(gè)concentration 保持不變,并不意味著所有的concentrations都相等!敲黑板!以上兩個(gè)方面也是考試中Why chemical equilibrium is a dynamic equilibrium 的答案!
Le chatelier’s principle 是幫助我們判斷化學(xué)反應(yīng)平衡移動(dòng)的重要規(guī)則,對(duì)于一個(gè)已經(jīng)達(dá)到平衡的可以反應(yīng),conditions 的改變就會(huì)引起化學(xué)反應(yīng)平衡的移動(dòng)。
能夠引起平衡移動(dòng)的factors小編相信同學(xué)們已經(jīng)非常熟悉了,它們分別是concentration, pressure(gaseous system),temperature (Endothermic or exothermic), 最后一個(gè)就是catalyst。
對(duì)于前面幾個(gè),相信同學(xué)們已經(jīng)能夠很好的判斷平衡移動(dòng)的方向了,在這兒小編要著重給同學(xué)們講講最后一個(gè)catalyst。
Catalyst并不能夠引起平衡的移動(dòng),它只是可以讓一個(gè)reaction能夠快速的達(dá)到平衡狀態(tài)。
當(dāng)然,我們?cè)趯W(xué)習(xí)catalyst的時(shí)候就提到過(guò),并不是所有加catalyst的目的都是加速reaction,也有一些reaction 需要減慢速度,只是我們平時(shí)不常見(jiàn)而已。
一般在catalyst當(dāng)中都有一個(gè)重要的組成部分,那就是transition metal,如果看到這個(gè)詞,同學(xué)們腦海中一片空白的話,快去翻翻書,把這部分知識(shí)撿起來(lái)! 因?yàn)榘凑招碌某鲱}的趨勢(shì),各個(gè)topic之間的聯(lián)系越來(lái)越大。
在一道題目中,只要能夠涉及的知識(shí)點(diǎn)都非常有可能考到。
在A2階段,這部分知識(shí)更是需要我們做更多的了解和學(xué)習(xí)。
首先就是一個(gè)量化的概念:Equilibrium constant
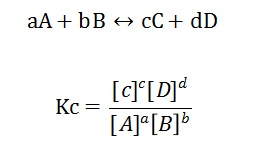
Kc就是這個(gè)reversible reaction的Equilibrium constant,[ ]代表這一個(gè)substance的concentration, 而a,b,c,d 則是這個(gè)reaction的balancing number。
注意!在記憶這個(gè)公式的時(shí)候一定要把它和rate equation 的計(jì)算公式區(qū)分開(kāi)(order of the reaction)。
當(dāng)然如果我們上面的ABCD都是Gas,那么這個(gè)Equilibrium constant也可以用Kp的形式來(lái)表達(dá):
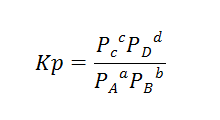
這里面,等等這些參數(shù)都是Partial pressure, 他們加起來(lái)就應(yīng)該是整個(gè)這個(gè)system的total pressure 。
那么這樣的話其實(shí)每一個(gè)partial pressure就非常好求啦,只需要用他們各自的fractional moles 去乘以total pressure 得到的就是每個(gè)substance各自的partial pressure.注意!
重點(diǎn)和易錯(cuò)的地方又來(lái)了,無(wú)論是Kc 還是Kp的計(jì)算,里面所用的concentration 和 partial pressure都是各個(gè)substance 在equilibrium 時(shí)候的value.也就是說(shuō)我們要以計(jì)算的value,既不是start of the reaction 時(shí)候的,也不是during the reaction 的!在這里再次強(qiáng)調(diào)是因?yàn)橥瑢W(xué)們經(jīng)常會(huì)在這里犯錯(cuò)而導(dǎo)致無(wú)謂的丟分。
一般來(lái)講,對(duì)于一個(gè)excess reactant,equilibrium concentration往往是它after reaction 剩下的,而對(duì)于product 而言,equilibrium concentration 往往是它after the reaction 生成的。
小編在這兒再次提醒同學(xué)們?cè)谟?jì)算的時(shí)候盡量按照標(biāo)準(zhǔn)的三段式進(jìn)行分析計(jì)算,即把start of the reaction, during the reaction 以及 equilibrium 這三個(gè)階段的concentration都寫在reaction 下面,然后所有的東西就都一目了然啦!
如果上面三個(gè)知識(shí)點(diǎn)同學(xué)們已經(jīng)掌握的非常棒了,那我們就來(lái)看看最有一個(gè)問(wèn)題,why le chatelier’s principle? ?不知道同學(xué)們是否想過(guò),我們可以用le chatelier’s principle 來(lái)判斷一個(gè)equilibrium 的移動(dòng)方向,但是為什么可以這樣,有沒(méi)有任何的theory可以支持這樣的一個(gè)規(guī)則呢?
答案當(dāng)然是肯定的,那就是我們上面講的這個(gè)equilibrium constant. 注意,Kc 和Kp只受溫度的影響,那么也就是說(shuō)在溫度不變的情況下,Kc 和Kp 是不變的!
那這樣的結(jié)論為什么能夠支持Le chatelier’s principle? 下面小編就為大家舉個(gè)例子,讓大家體驗(yàn)一下Equilibrium 的神奇。
我們就拿
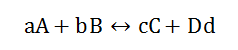
這個(gè)reaction來(lái)舉例,如果現(xiàn)在Increase the concentration of A, 我們先不著急用Le chatelier’s principle來(lái)判斷移動(dòng)方向,我們先看看Kc 這時(shí)候會(huì)有什么變化
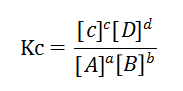
[A]如果突然增加,那么對(duì)于Kc來(lái)講會(huì)馬上decreace,形成一個(gè)新的Kc‘<Kc,我們說(shuō)過(guò)當(dāng)溫度不變時(shí),Kc是不變的,所以Kc’要變回到原來(lái)的Kc。
從數(shù)學(xué)角度來(lái)說(shuō),Kc’ 可以走的路有兩條:一.讓[B]decrease;二.讓[C] ,[D] increase. 那我們?cè)購(gòu)腸hemical reaction 的角度來(lái)看看,[B]decrease; [C] ,[D] increase, 是不是剛剛好是讓Equilibrium shifts to right 來(lái)實(shí)現(xiàn)的呢?
是不是剛剛好obey Le chatelier’s principle 呢?如果同學(xué)們有興趣,可以自己去試試別的conditions,屢試不爽。
最后一次敲黑板!在新的出題模式下,這種題目類型是考官特別喜歡的!

最新發(fā)布
? 2026. All Rights Reserved. 滬ICP備2023009024號(hào)-1









